一、AAV滴度的类型
颗粒滴度(Particle Titer):统计AAV完整颗粒的数量,包括有基因组的和“空壳”颗粒。
感染滴度(Infectious Titer):反映AAV实际进入并感染靶细胞能力的病毒数量。
实际项目中,一种AAV样品的基因组滴度、颗粒滴度、感染滴度可能有明显差异,合理选择和理解检测数据对实验至关重要。
二、AAV常用滴度检测方法对比
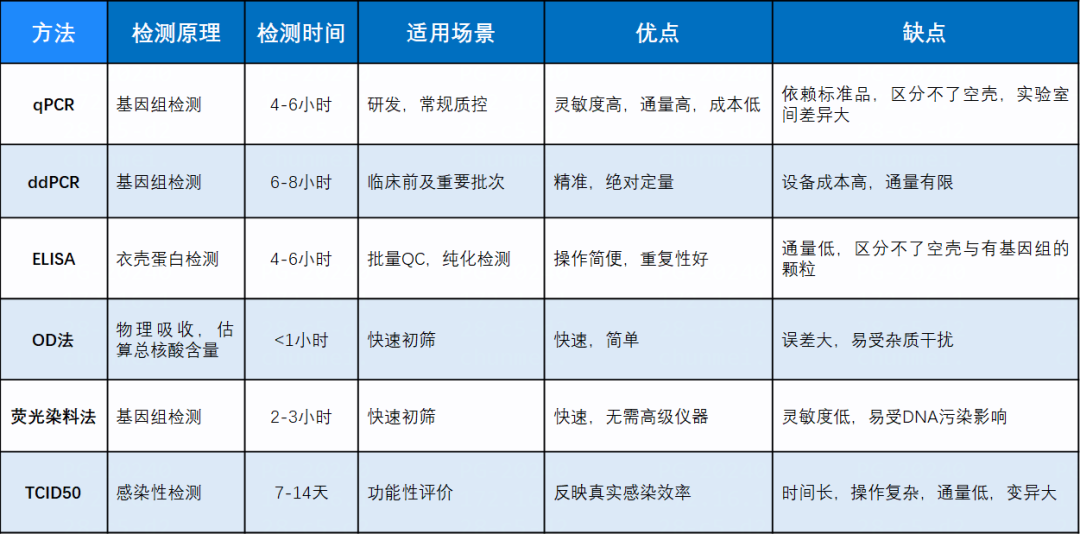
三、常见AAV滴度检测方法解析
原理:该方法通过特异性引物和探针扩增病毒基因组特定区域,并实时监测荧光信号强度来定量病毒基因组。常用的靶序列包括ITR区域、载体中的启动子或转基因序列等。
应用场景:
- AAV的生产研发;
- 早期工艺开发;
- 常规质控。
优点:
- 灵敏度高,可检测低至数百拷贝的基因组;
- 通量大,适用于批量样品检测;
- 操作流程成熟,试剂易得,设备在多数实验室已经普及。
缺点:
- 需高质量DNA标准品,引物设计要求高,可能导致系统性误差;
- 易受样品中PCR抑制剂的影响;
- 实验室间差异较大,重现性通常为70-100%CV;
- 难以区分空壳病毒和实心病毒。
注:重复性 (repeatability)和重现性 (reproducibility)是评价检测方法可靠性的两个关键指标。
重复性
定义:重复性是指在相同条件下,同一操作者使用相同设备,在短时间内对同一样品进行重复测量所获得结果的一致性。
具体表现:
- 同一实验室内
- 同一操作人员
- 相同的仪器设备
- 相同的试剂批次
- 短时间内完成(通常在同一天)
评价指标:通常用变异系数(CV%)表示,计算公式为标准差除以平均值再乘以100%。
实例:例如,在AAV滴度检测中,qPCR方法的重复性CV通常为10-50%,而ddPCR方法的重复性CV可达到2-30%,这意味着ddPCR在同一实验条件下的结果更加稳定。
重现性
定义:重现性是指在不同条件下,如不同实验室、不同操作者、不同设备对同一样品进行测量所获得结果的一致性。
具体表现:
- 不同实验室之间
- 不同操作人员
- 不同的仪器设备
- 不同的试剂批次
- 可能在不同的时间段完成
评价指标:同样用CV%表示,但重现性CV值通常大于重复性CV值。
实例:在AAV滴度测定中,qPCR的实验室间重现性CV可高达70-100%,这意味着不同实验室使用相同方法检测同一样品可能会得到相差一倍以上的结果。相比之下,ddPCR的重现性更好,主要是因为它采用绝对定量,无需依赖标准曲线。
2. ddPCR法(微滴式数字PCR)
原理:ddPCR将反应混合物分散成数万个微滴反应器,每个微滴中进行独立PCR扩增,最后通过计数阳性微滴的数量进行绝对定量,无需依赖标准曲线。
应用场景:
- 需要高精度定量的样品检测;
- 临床前、临床、商业化产品放行前检测;
- 参比标准品的制备。
优点:
- 绝对定量,无需标准曲线,减少系统误差;
- 重复性优于qPCR,为2-30%CV;
- 对PCR抑制剂的耐受性更好;
- 不同实验室间的一致性更高。
缺点:
- 设备成本高;
- 检测通量有限;
- 操作步骤相对复杂;
- 整体成本高于qPCR 。
3. 荧光染料法
原理:利用对DNA高度特异的荧光染料(如PicoGreen、SYBR Gold等)与纯化后的AAV样品中的病毒基因组结合,通过测量荧光强度来定量AAV基因组。
应用场景:
- 快速初筛;
- 高纯度样品的常规检测。
优点:
- 操作简单快速,2-3小时内完成;
- 成本较低。
缺点:
- 对样品纯度要求高,DNA污染会导致结果偏高;
- 灵敏度低于PCR方法;
- 不适用于复杂基质中的AAV检测。
基于蛋白的检测方法
1. ELISA法(酶联免疫吸附测定)
原理:利用特异性抗体识别AAV衣壳蛋白,通过酶联免疫反应检测AAV颗粒的数量。
应用场景:
- 生产过程中的质控检测;
- 纯化后产品的病毒颗粒数测定;
- 空壳率评估(与PCR方法结合使用)。
优点:
- 特异性强,只检测特异性抗体相应的衣壳;
- 对基质干扰相对不敏感;
- 操作相对标准化,商业试剂盒可用 。
缺点:
- 通量低(96孔板仅可测10个样品);
- 样品消耗大;
- 操作耗时(数小时);
- 重复性为10-15%CV,重现性约40%CV 。
2. 光学密度法(OD)
原理:根据蛋白质与核酸在260nm处的吸光度来估算AAV颗粒数量。针对高纯度的、空壳较少的AAV制剂,1×1012 vg/mL对应约OD260≈1。
应用场景:
- 高纯度AAV样品的快速检测;
- 生产过程中的粗略估计。
优点:
- 操作极为简单快速;
- 无需特殊设备,普通分光光度计即可;
- 成本低廉 。
缺点:
- 易受DNA和蛋白质杂质影响;
- 灵敏度低,不适用于低纯度样品;
- 无法区分空壳和实心颗粒。
功能滴度检测方法
原理:通过检测AAV感染细胞后的功能效应(如报告基因表达或辅助病毒共感染后的细胞病变)来测定具有感染能力的AAV颗粒数量。
应用场景:
- 需评估AAV感染活性的场合;
- 临床前和临床产品的感染活性检测。
优点:
- 直接反映AAV的感染活性;
- 可区分具有感染能力和无感染能力的颗粒;
- 结果与临床疗效相关性更高。
缺点:
- 检测周期长(7-14天);
- 人力资源消耗大;
- 结果受多种因素影响,变异较大。
新兴检测技术
近年来,一些新兴技术如Gyrolab微流体免疫分析平台和CRISPR诊断技术也被应用于AAV滴度检测。Gyrolab技术相比传统ELISA具有线性范围宽(提高2个对数级)、样品消耗少、通量高等优势,而CRISPR诊断技术则有望提供比qPCR更稳健的定量方法。
四、方法选择建议
1. 研发阶段:qPCR、ddPCR和ELISA的组合使用,全面了解AAV的基因组滴度、衣壳滴度以及空壳比例。
2. 生产过程控制:根据不同生产阶段,可选择qPCR和快速ELISA方法,平衡速度和准确性需求。
3. 产品放行:建议使用多种互补方法,如ddPCR确定基因组滴度,ELISA确定衣壳滴度,必要时进行功能性测定以确保产品质量。
4. 稳定性研究:选择重复性好的方法如ddPCR,确保数据可靠性。
AAV滴度的准确检测,是病毒载体开发与应用的基础。不同检测方法各有优缺点,没有“一刀切”的方案,合理组合使用可实现更全面的质量控制。
作为AAV包装与生产服务的专业企业,我们拥有完善的滴度检测平台,可以根据客户需求提供从qPCR、ddPCR、ELISA到TCID50等多种检测服务,确保您获得准确可靠的AAV滴度数据,为您的研究和临床应用保驾护航。
想了解更多AAV相关知识或获取服务支持,欢迎咨询我们或者留言。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。