
长期使用抗精神病药是导致心肌损伤甚至心源性猝死的常见原因。抗精神病药物的心脏毒性常导致停药或治疗中断。目前,关于抗精神病药物引起心脏毒性的具体机制尚不完全清楚,需要进一步的研究来阐明。

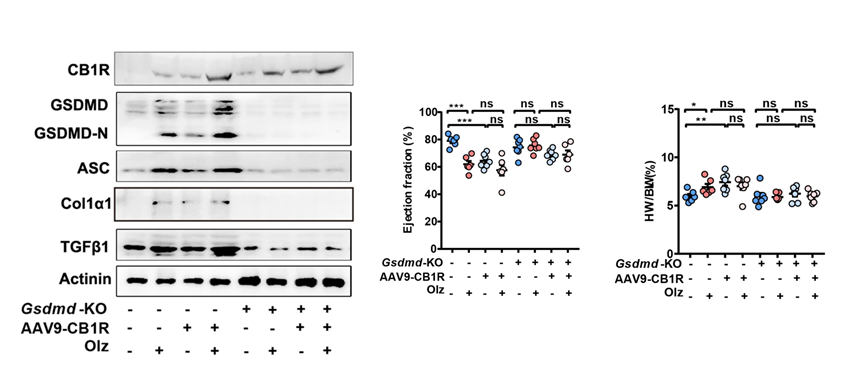
图1 过表达Cb1r能诱导心脏细胞焦亡和促纤维化因子的表达
本篇文章AAV的导入方式:
| 实验动物 | Gsdmd−/− 或 Gsdmd-KO小鼠 |
| 血清型 | AAV9 |
| 注射方式 | 原位注射心脏左心室,3-5个位点 |
| 注射剂量 | 2×10^11 vg/只 |
| 检测时间 | 感染后6周 |
心力衰竭作为全球主要的死亡原因之一,与心肌细胞的更新能力有密切关系。在心肌梗死后,成人心脏的心肌细胞更新能力极低,导致心脏功能受损和病理性重构。Hippo信号通路是一个抑制性激酶级联反应,它在心肌梗塞后抑制心肌细胞的增殖和更新。猪的心血管系统与人类有重要的相似之处。

- AAV9递送Sav-shRNA(图2)在成年猪心肌细胞中诱导Hippo通路缺陷
- AAV9-Sav-shRNA基因疗法在正常的猪心脏中诱导心肌细胞增殖
- AAV9-Sav-shRNA在猪心肌梗死模型中改善了收缩功能
- AAV9-Sav-shRNA在猪心肌梗死模型中促进心肌细胞进入细胞周期和分裂
- AAV9-Sav-shRNA促进猪心脏中心肌细胞肌节的短暂解体
- AAV9-Sav-shRNA促进猪心脏在心肌梗死后的血管生成
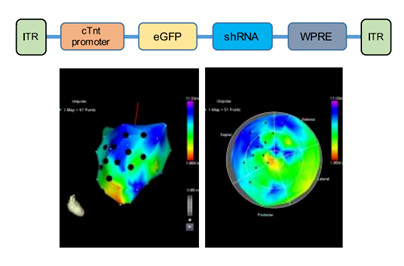
图12 AAV9-Sav-shRNA载体结构和导入位点示意图
本篇文章AAV的导入方式:
| 实验动物 | 猪 |
| 血清型 | AAV9 |
| 注射方式 | 心肌原位注射,10-15个位点 |
| 注射剂量 | 3.4×10^11 vg/kg |
| 检测时间 | 感染后4周 |
钙/钙调蛋白依赖性蛋白激酶IIδ(CaMKIIδ)是心脏信号传导和功能的核心调节器。然而,CaMKIIδ的慢性过度激活会导致人类和小鼠的多种心脏疾病,包括缺血/再灌注(IR)损伤、心力衰竭、肥大和心律失常。CaMKIIδ调节域中的两个甲硫氨酸残基,Met281和Met282的氧化,可以阻止催化域与自抑制区域的结合,促进激酶的超激活,而将这些甲硫氨酸残基修改为其他氨基酸可以防止氧化和CaMKIIδ的过度激活,从而提供心脏保护。

实验设计和主要研究结果:
- 碱基编辑系统的设计和sgRNA的筛选
- 碱基编辑的特异性研究:在人类iPSCs中进行脱靶分析
- 对CaMKIIδ编辑的人类iPSC衍生心肌细胞进行功能分析
- 在缺血/再灌注(IR)小鼠模型体内编辑CaMKIIδ(图3)
- 体内碱基编辑的编辑效率及潜在脱靶位点分析
- CaMKIIδ体内编辑对心脏的保护作用及其长期效应机制研究
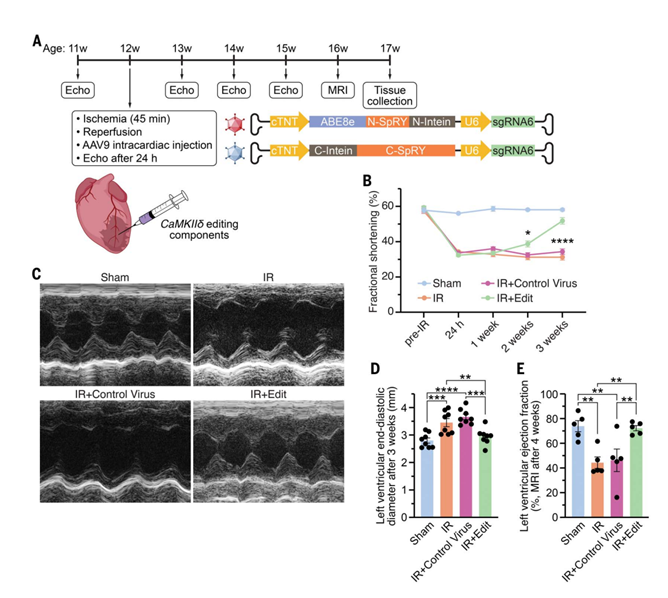
图3 体内CaMKIIδ碱基编辑改善了缺血/再灌注后的心脏功能
本篇文章AAV的导入方式:
| 实验动物 | 12周龄C57BL6小鼠 |
| 血清型 | AAV9 |
| 注射方式 | 心脏内注射,一次性注射30μL的剂量 |
| 注射剂量 | N- 和 C-term AAV9各注射7.5×10^11 vg/kg,共注射1.5×10^12 vg/kg |
| 检测时间 | 感染后2周 |
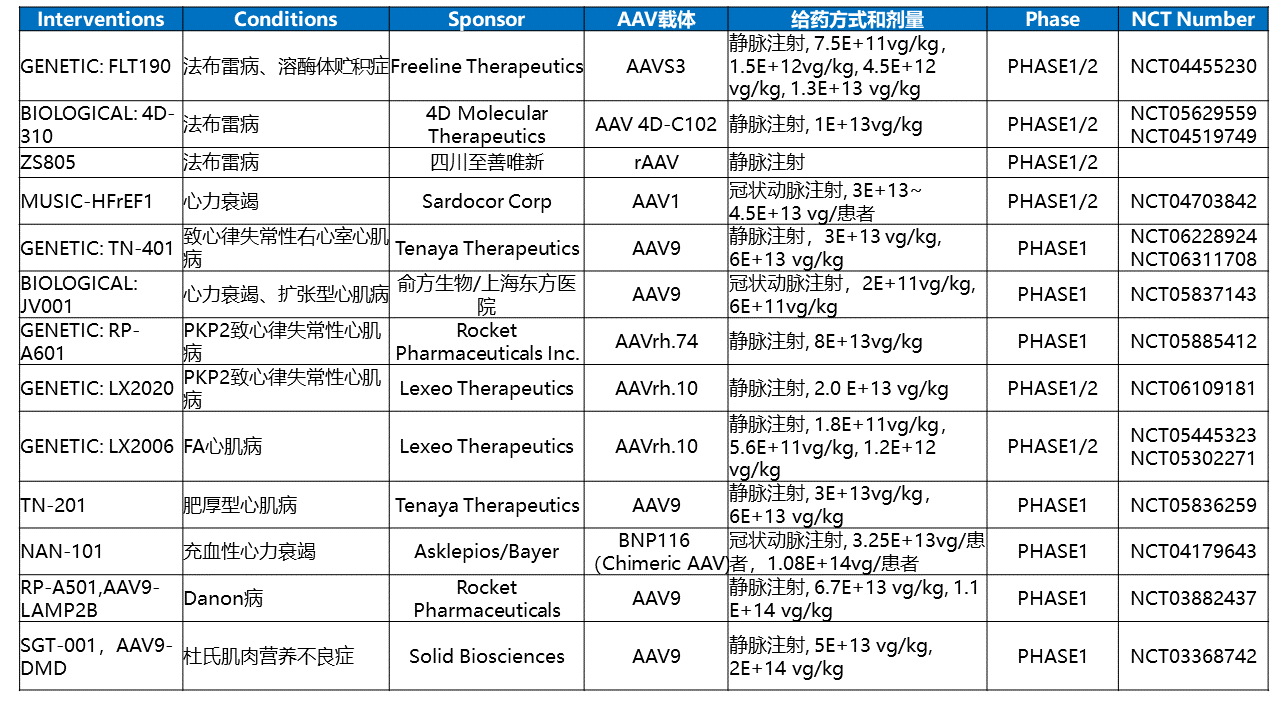
目前有多款基于AAV载体的心脏疾病基因治疗药物处于临床试验阶段(表1),适应症包括遗传性心肌病、心力衰竭和法布雷病等,主要的给药方式为静脉注射和冠状动脉注射。其中,临床试验进展较快的药物为Lexeo Therapeutics开发的LX2006。该药物已于2024年7月发布Ⅰ/Ⅱ临床试验结果。LX2006在基线左心室质量指数(LVMI)升高的FA心肌病患者中,LVMI在12个月时平均减少了11.4%,在18个月时减少了18.3%。在12个月时,大多数参与者的其他关键心脏状况指标,包括左心室壁厚度和肌钙蛋白I,持续得到改善,所有参与者的frataxin表达量在治疗后均高于基线。到目前为止,LX2006的耐受性良好,没有与治疗相关的严重不良事件4。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。

